肺癌患者参加临床试验早已经不是以前的新药“小白鼠”,而是可以让患者可以更早得到新药或者新治疗方案的重要方式。尤其是在目前成熟的伦理委员会的审核机制下,肺癌药物临床试验给患者带来获益有着很大的保证。
特别是对于一些新的靶向药物来说,可能在药物上市前患者就已经翘首以盼,这样临床研究中的提前使用可能对患者意味着难得的生存机会。不仅如此,对于经济条件一般的患者来说,即使药物上市后可能也无法负担每月数万的高昂费用,这样临床试验也能患者带来的经济上的减免(临床研究中的药物几乎全是免费的)。
但临床试验的入组条件往往比较苛刻,能入组的患者仅是很少一部分。为了保证临床研究的质量,尽可能得到阳性结果而保证药物顺利上市(这对于花费了大量研发费用的企业来说也无可厚非),临床研究开始前的筛选是一个比较严格的过程。患者必须满足所有的入组条件,才能纳入研究。某些病理切片,血液等指标也需要中心实验室的确认,这样必然会增加患者的等待时间,而一旦筛选失败,则反而会延误患者的治疗。
这样,在患者是否符合入组条件这个问题上,经常会发生我们研究者(医生)与申办方(药企)争论的情况。医生希望患者入组而得到药物治疗获得机会,而申办方而认为患者不符合入组条件,无法使患者入组。
在数年前某ALK靶向药物的临床研究中,本人也曾经为了争取患者的成功入组和申办方进行了数次沟通。原因是研究方案要求患者为化疗失败后的二线治疗,而该患者接受了一次化疗后因副作用大(并非疾病进展)更换过一次化疗药物,而被认为接受了二线化疗,不符合入组条件。最终患者没有能够加入研究,接受ALK新药的治疗。后续等待药物上市,患者已经没有机会使用了,这也让我非常遗憾。几乎每个临床研究,都会发生这样的争论。
基于这个明显的问题,FDA于2020年发布了“以患者为中心(patient-centric trials,PCT)”的临床研究指南,旨在扩大可以从临床研究中获益的患者人群。对于不符合入组条件的患者,采用“同情用药(CU)”的方式,把患者纳入临床研究中来。但至今,真正以患者为中心的临床研究仍很少。
而吴一龙教授最近发表在Nature medicine中的这项临床研究,为“以患者为中心”这个模式做出了表率。作为一个小样本的II期研究能发表于Nature medcine,本身也代表了对“以患者为中心”临床研究的这个模式的肯定。

DOI: 10.1038/s41591-023-02461-x
这项伞式研究纳入48例HER2 突变的患者,采用吡咯替尼靶向一线治疗。其中完全满足入组条件(CF)有28例患者,另外有12例患者不符合入组条件,仍按照“以患者为中心”入组给予同情用药(CU)。另有8例患者为真实世界用药(RWS)。
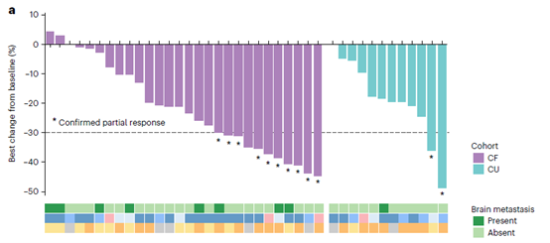
CF组缓解率为35.7%,同情用药(CU)组为15.7%。虽然同情用药组缓解率低于CF组,但是12例中11例83.4%患者肿瘤均有缩小。
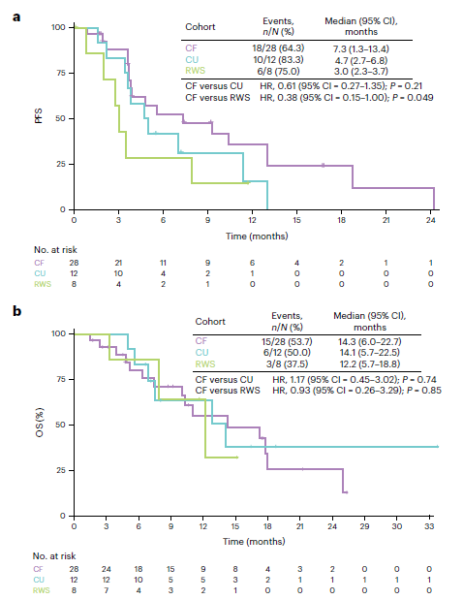
mPFS方面,CF组7.3月,CU组4.7月,RWS3.0个月。
mOS方面,CF14.3月,CU14.4月,RWS12.2月,3组基本类似。同情用药也可以获得OS获益。
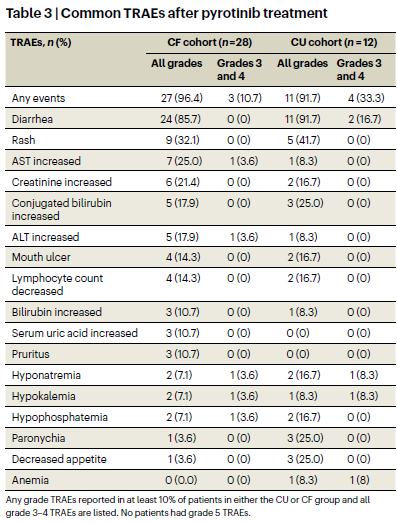
不良反应方面,CF组3-4级的不良反应总体为10.7%,而CU组3-4级不良反应为33.3%,确实有所轻微升高。包括腹泻,低钠血症和低钾血症。
本研究的意义在于给“以患者为中心”的临床研究提供了可行性示范。以便临床研究新药可以惠及更多的患者。在临床研究进行的同时,初步符合但筛选失败的患者,经医师讨论后设立“同情用药”亚组,这样既可以使临床研究顺利进行,也可以扩大获益人群。我们研究者热烈期盼更多的“以患者为中心”的临床研究问世。(作者,复旦大学附属中山医院呼吸科副主任医师,张勇)
注:请在转载文章内容时务必注明出处!
编辑:许兵




